Существует ряд различных вариантов инъекционного введения препаратов (ИВП) при боли в тазобедренном суставе (БТС), которые могут быть предложены пациентам. Несмотря на то, что ИВП может принести значительную пользу при БТС, важно знать о сопутствующих ограничениях и рисках. В каждом конкретном случае врачи должны рассматривать все возможные варианты и обсуждать их с пациентом в процессе совместного принятия решения.
ИВП при БТС может быть внутрисуставным (лекарства вводятся в тазобедренный сустав) или внесуставным — чаще всего препараты вводятся вокруг сухожилий. ИВП может проводиться с диагностической целью или для уменьшения БТС и восстановления трудоспособности. Что касается терапевтического эффекта, то ИВП, как правило, приносит лишь кратковременное облегчение (или облегчение в среднесрочной перспективе). Поэтому при проведении ИВП необходимо проводить обучение, направленное на оптимизацию результатов путем сочетания ИВП с более активными методами лечения, такими как лечебная физкультура и обучение управлению нагрузками.
Следует также внимательно рассмотреть вопрос о том, в каких случаях целесообразно использовать ИВП. Этот вариант часто предлагается в качестве первой линии лечения БТС, хотя это не подтверждается доказательствами и может быть связано с существенными рисками. Давайте рассмотрим, что нам известно на сегодняшний день.
Вот основные темы, которые мы будем обсуждать в этой статье:
- Общие риски ИВП при боли в тазобедренном суставе.
- Варианты, преимущества и риски инъекций в тазобедренный сустав.
- Варианты, преимущества и риски периартикулярных инъекций.
Общие риски ИВП при боли в тазобедренном суставе
Нежелательные явления при инъекциях в тазобедренный сустав варьируются от легких до более серьезных. Риски ИВП могут быть связаны с вводимым веществом, но инфекция или ятрогенное повреждение тканей могут возникнуть просто в результате процесса введения иглы в тазобедренный сустав или внесуставные мягкие ткани. Эти риски невелики, но все же они имеют место, поэтому мы рассмотрим их в первую очередь. Затем мы перейдем к обсуждению конкретных инъекций при БТС.
Аллергические реакции и инфекции
Хотя эти осложнения встречаются крайне редко, последствия аллергических реакций и инфекций варьируются от легких до чрезвычайно выраженных. Аллергические реакции могут проявляться в виде покраснения и зуда кожи, а некоторые люди могут реагировать на определенные вещества полной анафилаксией. Некоторые препараты содержат белки или другие аллергены, которые могут привести к анафилактическому шоку. Во избежание неблагоприятных исходов, связанных с этими побочными эффектами, пациенты должны быть соответствующим образом обследованы и какое-то время находиться под наблюдением после введения лекарства.
При ИВП для лечения БТС возможно занесение инфекции в кожу, периартикулярные мягкие ткани или тазобедренный сустав. Если кожные инфекции часто относительно легко поддаются лечению местными или пероральными антибиотиками, то «более глубокие» инфекции мягких тканей и особенно внутрисуставные инфекции могут быть весьма разрушительными. Септический артрит, вызванный внутрисуставной инъекцией, может привести к быстрому разрушению сустава, если воспалительный процесс не купировать на ранней стадии. Повторимся, что такие осложнения встречаются крайне редко.
Очень важен высокий уровень гигиены, как с точки зрения использования стерильного оборудования, так и с точки зрения подготовки кожи (требования асептики и антисептики). Также важен скрининг пациентов с кожными заболеваниями или инфекциями.
Локальное физическое повреждение тканей при введении иглы
Помимо аллергических реакций и инфекций, к общим рискам ИВП относится также относительно низкий риск ятрогенного повреждения тканей, что может возникнуть при введении иглы в тазобедренный сустав или мягкие ткани.
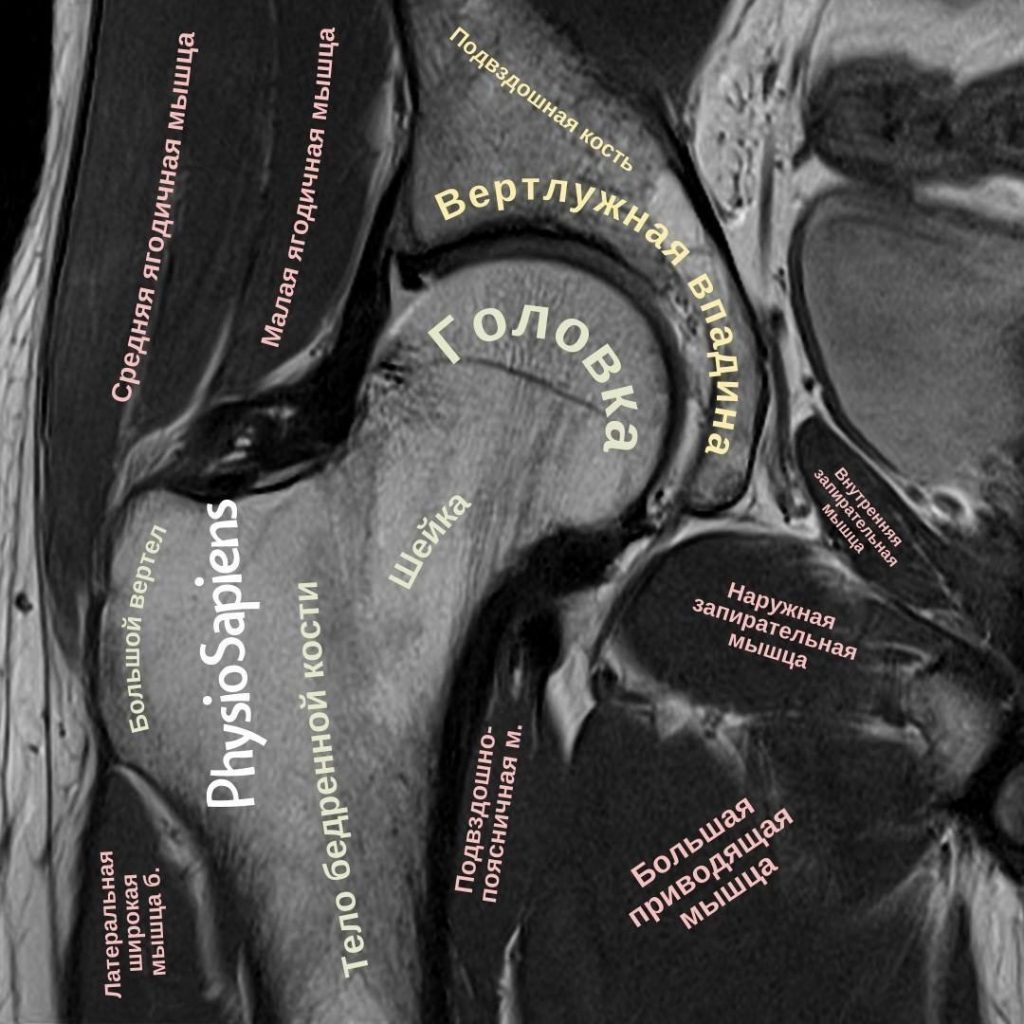
В частности, инъекции в тазобедренный сустав чаще всего выполняются под визуальным контролем, с помощью ультразвука, флюороскопии или компьютерной томографии (КТ). В некоторых случаях игла может задеть хрящ нижней части головки бедренной кости, но при инъекциях под визуализацией это случается редко (поскольку место инъекции находится в периферическом отсеке — в пределах капсулы, но на уровне шейки бедренной кости). Таким образом, при правильном расположении иглы ее кончик должен находиться на безопасном расстоянии от суставного хряща и вертлужной впадины.
Иногда из-за отсутствия доступа или в связи с временными и финансовыми трудностями инъекции могут выполняться «вслепую», ориентируясь для направления кончика иглы только на поверхностную анатомию. При выполнении инъекций вслепую существует повышенный риск неадекватного позиционирования кончика иглы в плане воздействия на целевую ткань и/или случайного попадания в смежные структуры (Diraçoğlu, 2009).
Потенциальным риском является травма сосудисто-нервного пучка, но в случае использования системы навигации это встречается редко. Случайный контакт с нервом или сосудом может привести к нейропатии или гематоме (Zhang, 2008). КТ или ультразвуковое наведение с допплерографией может помочь безопасно ввести иглу туда, где находятся важные сосудисто-нервные структуры, например, в области передней поверхности тазобедренного сустава (Diraçoğlu, 2009; Mezian, 2022) или в ишиофеморальном промежутке (Liou, 2023).
Лучевое воздействие, связанное с рентгеноскопией или инъекциями под контролем компьютерной томографии
Внутрисуставные инъекции обычно проводятся под контролем рентгеноскопии или компьютерной томографии. Оба этих метода визуализации включают ионизирующее излучение.
Рентгеноскопия включает в себя серию рентгеновских снимков для визуализации костных ориентиров в режиме реального времени. Каждое изображение имеет относительно низкую дозу облучения, однако доза облучения является кумулятивной, а длительность съемки определяет общее облучение. Продолжительность съемки увеличивается в зависимости от ИМТ, поэтому пациенты с ожирением могут подвергаться рентгеновскому воздействию длительностью 20-30 секунд, что представляет собой потенциально значительную дозу облучения.
Другим распространенным методом внутрисуставного введения иглы является КТ-визуализация. Она может использоваться для ИВП, аспирации или введения контраста для артрографии — обычно с последующей магнитно-резонансной томографией для оценки состояния сустава с контрастом — МР-артрограммой. При установке иглы делается КТ-снимок, вводится игла, а затем ее положение снова проверяется с помощью одного или нескольких КТ-снимков. При традиционном КТ-наведении пациент подвергается более высокому уровню облучения, чем при рентгеноскопии, хотя недавно были описаны новые протоколы со сверхнизкими дозами облучения (Goeller, 2021).
Однократная процедура визуализации несет минимальный риск последующих проблем со здоровьем, связанных с облучением, для соответствующим образом отобранных пациентов. Однако необходимо учитывать совокупный риск у тех, кому, возможно, предстоят повторные процедуры или визуализация различных частей тела. Это может быть более распространенным у пациентов с хроническими заболеваниями или спортсменов, занимающихся контактными видами спорта или другими видами спорта с высоким риском травматизма.
Инъекции под контролем ультразвука, как правило, предпочтительнее из-за отсутствия ионизирующего излучения, но эти процедуры требуют соответствующего оборудования и квалифицированного специалиста.
Варианты, преимущества и риски инъекций в тазобедренный сустав
При диагностике и лечении БТС врачи используют различные инъекции. К наиболее распространенным инъекциям относятся инъекции местных анестетиков и кортикостероидов, а в последнее время появились вискосуппозиции с гиалуроновой кислотой и инъекции богатой тромбоцитами плазмы. Давайте рассмотрим показания, механизмы, преимущества и побочные эффекты, связанные с этими вариантами инъекций в тазобедренный сустав.
Инъекции местных анестетиков
Показания и преимущества введения в тазобедренный сустав местных анестетиков
Внутрисуставные инъекции местных анестетиков чаще всего используются в диагностических целях. Это может быть показано при рассмотрении вопроса о хирургическом вмешательстве. Если во время действия анестетика симптомы не меняются, можно рассмотреть другие диагнозы и методы лечения или проконсультировать пациента, что шансы на хороший исход операции, скорее всего, снизятся.
В одном из недавних проспективных исследований пациентам с БТС предлагалось выполнить ряд провокационных функциональных тестов (ходьба на беговой дорожке, боковые шаги вниз, прыжковые тесты) до и после внутрисуставной инъекции местного анестетика. Результаты 90 пациентов, которым впоследствии была проведена артроскопическая операция, отслеживались в течение 12 месяцев. У тех, кто испытывал менее 75% уменьшения боли при выполнении батареи провокационных функциональных тестов, исход был хуже, чем у тех, кто отмечал 75% и более уменьшения симптомов при предоперационном тестировании (Haws, 2022).
Местный анестетик также часто добавляют к кортикостероиду для оценки немедленного эффекта от внутрисуставной инъекции.
Для диагностических целей важно, чтобы инъекционный препарат был точно введен в тазобедренный сустав и не вытекал за его пределы. Неправильное расположение или экстравазация во внесуставные ткани снижают точность диагностики, поскольку положительный эффект может быть обусловлен воздействием на внесуставные ткани. Примерно у 15% людей тазобедренный сустав сообщается с бурсой подвздошно-поясничной мышцы (Hirji, 2011), поэтому внутрисуставное введение анестетика может уменьшить боль, связанную с этой бурсой.
Возможные риски при внутрисуставном введении местного анестетика
Исследования показали, что местные анестетики, такие как Лидокаин и Бупивакаин, являются хондротоксичными — токсичными для клеток хряща. Местные анестетики могут влиять на жизнеспособность хондроцитов, подавлять синтез матрикса и способствовать апоптозу хондроцитов (запрограммированной гибели клеток).
Степень этого воздействия зависит от конкретного местного анестетика, концентрации и длительности воздействия.
В целом, по имеющимся данным:
- Лидокаин и Бупивакаин обладают наибольшей хондротоксичностью;
- более высокие концентрации Лидокаина и Бупивакаина (т.е. 2% против 1% и 0,5% против 0,25%) более токсичны для хондроцитов;
- бОльшая экспозиция более токсична.
Воздействие местных анестетиков на хрящ в течение более 1 часа приводит к значительному негативному воздействию на хондроциты in vitro. Период полураспада распространенных местных анестетиков составляет от 1,6 до 3,5 часов, причем Бупивакаин имеет самый длительный период полураспада — 3,5 часа (Zhang, 2023).
Более длительное время воздействия также может быть связано с наличием внутрисуставного катетера, который иногда оставляют в суставе на некоторое время для обезболивания в послеоперационный период. Это может вызвать гораздо большую токсичность для хряща, чем однократная внутрисуставная инъекция (Piper, 2011; Lemos, 2022). Действительно, у некоторых людей после использования внутрисуставных местных анестетиков после артроскопии плечевого и коленного суставов наблюдался хондролиз — полное разрушение суставного хряща (Zhang, 2023).
Кроме того, необходимо учитывать эффект смешивания инъекционных препаратов. Добавление кортикостероида к инъекции местного анестетика, по-видимому, усиливает хондротоксическое действие (Piper, 2011; Lemos, 2022). Такая комбинация часто встречается при внутрисуставных инъекциях, выполняющихся для уменьшения БТС.
Исходя из имеющихся данных, внутрисуставные местные анестетики должны применяться с осторожностью, с минимально возможными концентрациями и экспозицией. Вместо Бупивакаина и Лидокаина рекомендуется использовать Ропивакаин и Мепивакаин, поскольку они менее токсичны для хряща (Zhang, 2023).
Инъекции кортикостероидов
Показания, механизмы и преимущества введения в тазобедренный сустав кортикостероидов
Инъекции кортикостероидов, также известные как инъекции Кортизона, часто используются для купирования боли и уменьшения воспаления в тазобедренном суставе. Кортикостероиды, такие как Метилпреднизолон или Триамцинолон, обладают мощным противовоспалительным и иммуносупрессивным действием (Ayhan, 2014).
Кортикостероиды прерывают воспалительный и иммунный каскад на нескольких уровнях. Они уменьшают проницаемость сосудов, препятствуют накоплению воспалительных клеток, предотвращают синтез и секрецию ряда медиаторов воспаления, таких как простагландины и лейкотриены (Ayhan, 2014).
Внутрисуставное введение кортикостероидов раньше использовалось в основном при лечении остеоартрита тазобедренного сустава, однако в последние годы, по-видимому, все чаще инъекционные препараты применяются у более молодых пациентов с фемороацетабулярным импинджментом, дисплазией и разрывами суставной губы.
Многие исследования показали кратковременный обезболивающий эффект инъекций кортикостероидов для пациентов с остеоартритом тазобедренного сустава. В недавнем систематическом обзоре и мета-анализе внутрисуставных инъекций в тазобедренный сустав сообщается, что кортикостероиды являются наиболее эффективными в краткосрочной перспективе (1 месяц), однако в среднесрочной и долгосрочной перспективе (3 месяца и более) эти преимущества обычно теряются (Zhao, 2019).
Еще один недавний систематический обзор и мета-анализ рандомизированных контролируемых исследований, включавших внутрисуставные инъекции плацебо-солевого раствора, показал, что как по болевым, так и по функциональным результатам внутрисуставных инъекций при остеоартрите тазобедренного сустава ни одно из вмешательств (включая кортикостероиды) не превосходило по эффективности инъекции плацебо в период до 6 месяцев. Интересно, что изменения по сравнению с исходным уровнем превышали минимальные клинически значимые различия как при введении кортикостероидов, так и плацебо, что снижает ясность в отношении механизма эффекта (Gazendam, 2021).
Еще один систематический обзор и мета-анализ результатов неоперативного лечения при БТС суставе без артрита (например, фемороацетабулярного импинджмент-синдрома, дисплазии вертлужной впадины, разрыва суставной губы) выявил мало доказательств в пользу применения внутрисуставных кортикостероидов у пациентов без артрита. Они с очень низкой степенью достоверности подтвердили уменьшение боли и улучшение функции в течение 12 недель (Probst, 2023).
Таким образом, несмотря на наличие доказательств того, что внутрисуставные инъекции Кортизона могут способствовать уменьшению боли и улучшению функции у пациентов с остеоартритом тазобедренного сустава, эти эффекты кратковременны и должны быть сопоставлены с потенциальными рисками. Доказательства в пользу применения внутрисуставных кортикостероидов у пациентов с неартритическими болями в тазобедренном суставе в настоящее время слабы, и, возможно, большее беспокойство вызывают следующие побочные эффекты.
Возможные риски при внутрисуставном введении кортикостероидов
В научных исследованиях сообщалось о ряде побочных эффектов внутрисуставных инъекций кортикостероидов, включая повреждение хряща, аваскулярный некроз и воспаление сустава и последующее протезирование.
Кортикостероиды, хондротоксичность, аваскулярный некроз и быстроразвивающийся остеоартрит
Как и в случае инъекций местных анестетиков, исследования in vitro и in vivo на животных показали, что кортикостероиды оказывают токсическое действие на клетки хряща, приводя к значительной хондротоксичности и гибели клеток (Wernecke, 2015). Эффект еще более усиливается, если Кортизон вводится в паре с местным анестетиком (Piper, 2011; Lemos, 2022), что часто встречается в клинической практике. Кортикостероиды также токсичны для клеток костной ткани, поэтому прием высоких доз пероральных стероидов или повторные внутрисуставные инъекции могут повысить риск развития аваскулярного некроза головки бедренной кости.
Исследование Kompel и соавт. в 2019 г. вызвало беспокойство, когда они сообщили о четырех основных неблагоприятных результатах, наблюдавшихся у пациентов после внутрисуставных инъекций кортикостероидов: ускоренное прогрессирование остеоартрита (6%), перелом субхондральной кости (0,9%), аваскулярный некроз (остеонекроз) (0,7%) и быстрое разрушение сустава, включая поражение кости (0,7%).
В другом исследовании (Simeone, 2019) проводился слепой анализ повторных рентгенограмм пациентов, которым были или не были сделаны внутрисуставные инъекции Кортизона. Прогрессирование остеоартрита в течение 3-12 месяцев наблюдалось у 24% пациентов, которым инъекции не проводились, и у 44% пациентов, которым вводился Кортизон. При этом разрушение сустава произошло только у 1% пациентов, которым не выполняли ИВП, и у 17% которым вводили Кортизон.
Kompel и соавторы (2019) обнаружили, что серьезные нежелательные явления после инъекций кортикостероидов чаще возникают у пациентов с уже существующим аваскулярным некрозом, переломом с субхондральной недостаточностью или на очень ранних стадиях быстро прогрессирующего остеоартрита тазобедренного сустава.
Другое недавнее ретроспективное исследование показало, что если исключить из анализа пациентов с уже существующим аваскулярным некрозом и переломом с субхондральной недостаточностью, то у пациентов, которым вводили кортикостероиды, не наблюдалось достоверно более высоких показателей краткосрочного прогрессирования остеоартрита тазобедренного сустава или разрушения суставной поверхности головки бедренной кости (Abraham, 2021).
Таким образом, представляется крайне важным, чтобы пациенты с такими предсуществующими факторами риска были выявлены до начала внутрисуставного введения кортикостероидов. Перелом с субхондральной недостаточностью и остеонекроз иногда можно диагностировать с помощью рентгенографии, хотя изменения могут быть малозаметны или не видны на рентгенограмме. Поэтому эти факторы риска часто, к сожалению, легко упускаются.
Факторы риска, на которые следует обратить внимание
Лица, подверженные риску развития более тяжелых побочных эффектов после внутрисуставного введения кортикостероидов:
- пожилой возраст, белая раса;
- лица с предсуществующим аваскулярным некрозом:
- вторичный по отношению к травме и нарушению кровоснабжения — шейка бедра или вывих;
- нетравматическое внезапное начало боли, с возможным анамнезом:
- длительный прием пероральных стероидов;
- длительное злоупотребление алкоголем;
- лучевая терапия или химиотерапия;
- другие состояния здоровья — заболевания крови, аутоиммунные нарушения, ВИЧ и т.д.
- лица с ранее существовавшим переломом с субхондральной недостаточностью:
- пожилой человек с остеопорозом;
- молодой взрослый, ведущий активный образ жизни;
- острая боль, постепенно усиливающаяся в течение нескольких недель без какого-либо идентифицируемого инцидента;
- ультразвуковые данные, такие как больший, чем ожидалось, суставной выпот, обширные внутрисуставные обломки или утолщение синовиальной оболочки, указывающие на активный процесс в суставе.
- больные с быстро прогрессирующей формой остеоартрита (Kompel, 2019).
Скрининг:
Если боль достаточно сильная, перед инъекцией может потребоваться рентгенография или УЗИ. Если на рентгенограмме при высоком уровне боли не выявлено минимальных изменений в суставе, то для исключения перелома и выявления ранних признаков быстро прогрессирующего остеоартрита тазобедренного сустава (выпот в суставе, синовит, изменения прилегающих мягких тканей, отек субхондрального костного мозга) может быть показана МРТ. МРТ также помогает лучше выявить аваскулярный некроз (остеонекроз) головки бедренной кости.
Важно тщательно учитывать эти факторы риска. Кортикостероиды препятствуют заживлению костей, а уменьшение боли в суставах может привести к увеличению нагрузки, что в совокупности может привести к разрушению костей и суставов у пациентов с субхондральной недостаточностью, аваскулярным некрозом или быстро прогрессирующим остеоартритом тазобедренного сустава.
Кортикостероиды и воспаление нативного или протезированного тазобедренного сустава
Внутрисуставные инъекции кортикостероидов сопряжены с риском инфицирования сустава и развития септического артрита, хотя этот риск очень низок при соблюдении асептики и антисептики и обследовании пациентов с кожными инфекциями или предрасполагающими дерматологическими заболеваниями.
Большую озабоченность вызывает возможный повышенный риск развития перипротезной инфекции у тех, кто недавно перенес предоперационную внутрисуставную инъекцию Кортизона. Иммуносупрессивное действие кортикостероидов может не только повышать риск инфекции, но и препятствовать остеоинтеграции бесцементного протеза в раннем послеоперационном периоде (Gerhardt, 2020).
Перипротезные инфекции суставов +/- отсутствие остеоинтеграции могут быть губительными, приводя к ранним ревизионным операциям на суставах с худшими результатами, гораздо более высокой частотой послеоперационных осложнений и большими затратами.
В двух систематических обзорах с мета-анализом (Avila, 2023; Albanese, 2023) было установлено, что у пациентов, которым выполняли предоперационные инъекции кортикостероидов в течение 3 месяцев до тотального эндопротезирования тазобедренного сустава, риск развития перипротезной инфекции оказался значительно выше. В обоих случаях ученые рекомендовали пациентам, нуждающимся в тотальном эндопротезировании тазобедренного сустава, выждать не менее 3 месяцев после внутрисуставного введения кортикостероидов, чтобы снизить риск развития послеоперационной инфекции.
Этот вывод делает еще более важным адекватное обследование пациентов на предмет выявления факторов риска, которые могут привести к быстрому разрушению сустава после введения кортикостероидов. Для тех, кто столкнулся с подобными неблагоприятными явлениями, в случае необходимости быстрого перехода к хирургической замене сустава возникает дополнительный риск развития перипротезной инфекции.
Учитывая возможность повреждения хондральной ткани и такое разрушительное развитие событий, целесообразно сначала рассмотреть альтернативные методы лечения боли в тазобедренном суставе. При использовании инъекций целесообразно проводить тщательный скрининг пациентов с остеоартритом легкой степени и предоперационное планирование для пациентов с остеоартритом на поздней стадии (не проводить инъекции в течение 3 месяцев после планируемой операции).
Инъекции вискосуппозита
Показания, механизмы и преимущества инъекций в тазобедренный сустав вискосуппозита
Вискосуппозиция предполагает внутрисуставное введение гиалуроновой кислоты. Гиалуроновая кислота — вещество естественного происхождения, содержащееся в синовиальной жидкости суставов. Это высокомолекулярный гликозаминогликан, играющий ключевую роль в поддержании смазки суставов, вязкости и амортизирующих свойств синовиальной жидкости.
В последние годы вискосуппозиции приобрели популярность как метод лечения остеоартрита тазобедренного сустава и даже купирования болевого синдрома в тазобедренном суставе у молодых людей. Гиалуроновая кислота производится либо из петушиных гребней, либо путем бактериальной ферментации in vitro (Ayhan, 2014). Распространенные торговые названия: Durolane, Synvisc, Monovisc и Euflexxa.
Воспаление, связанное с остеоартритом, приводит к повышению проницаемости синовиальной мембраны для гиалуроновой кислоты. Повышенный уровень воспалительных цитокинов, свободных радикалов и протеолитических ферментов в остеоартрозных суставах также нарушает нормальное функционирование гиалуроновой кислоты и способствует прогрессированию остеоартрита. Эти воспалительные процессы приводят к снижению концентрации и молекулярной массы естественной гиалуроновой кислоты (Ayhan, 2014).
Сама жидкость при инъекциях становится вязкой, и считается, что вискодобавки временно восстанавливают вязкоупругие свойства и, следовательно, смазывающий и амортизирующий эффект синовиальной жидкости. Предполагаются и другие эффекты, в том числе уменьшение воспаления синовиальной оболочки, защита от эрозии хряща и стимуляция выработки эндогенной гиалуроновой кислоты, хотя эти эффекты не вполне доказаны (Ayhan, 2014).
Гиалуроновая кислота также имеет два потенциальных механизма обезболивания — непрямой через противовоспалительные свойства и прямой через ингибирование ноцицепторов и синтез брадикинина и субстанции Р (Ayhan, 2014).
Несмотря на перспективность этих потенциальных механизмов действия, данные о гиалуроновой кислоте неоднозначны: в одних исследованиях эффект отсутствует, в других — отмечается положительный эффект в краткосрочной и среднесрочной перспективе. Мета-анализ, проведенный Probst в 2020 году показал, что гиалуроновая кислота уменьшает боль в большей степени, чем контрольная инъекция (обычно физиологического раствора) через 1 и 3 месяца, но не через 6 месяцев. Инъекции кортикостероидов были более эффективны, чем гиалуроновая кислота в 1-месячный срок.
Что касается функционального эффекта, то через 2 месяца после инъекции гиалуроновая кислота превосходила контрольную инъекцию и была равна инъекции кортикостероидов с точки зрения улучшения показателей по шкале WOMAC. По данным обзора Zhao (2023) протоколы инъекций различались, но в целом инъекции гиалуроновой кислоты в тазобедренный сустав при остеоартрите приводили к уменьшению боли и, в меньшей степени, к улучшению функции, а также к сокращению перорального применения противовоспалительных средств (доказательность от очень низкой до низкой).
Эффект часто бывает более отсроченным, чем при использовании местных анестетиков и кортикостероидов: обычно ожидается, что он наступит через несколько недель. Однако улучшения отмечались уже через 2 недели, а в некоторых случаях они сохранялись до 12 месяцев после инъекции (Zhao, 2023).
Возможные риски при внутрисуставных инъекциях вискосуппозита в тазобедренный сустав
В отличие от местных анестетиков и кортикостероидов, гиалуроновая кислота не токсична для клеток хряща. Она безопасна для применения у пациентов с остеоартритом, единственным значимым побочным эффектом являются преходящие местные реакции в суставе, куда вводится препарат (у 2-4% пациентов) (Ayhan, 2014). Однако иногда к инъекции гиалуроновой кислоты добавляют кортикостероид. Это сопряжено с риском, связанным с введением кортикостероидов.
Инъекции богатой тромбоцитами плазмы
Показания, механизмы и преимущества инъекций в тазобедренный сустав богатой тромбоцитами плазмы
Инъекции богатой тромбоцитами плазмы (PRP) быстро завоевали популярность в качестве метода лечения различных заболеваний суставов и мягких тканей. Эта популярность несколько снизилась после того, как систематические обзоры показали незначительный эффект, а в разных странах было прекращено государственное финансирование этого вмешательства. Однако PRP продолжает оставаться одним из вариантов лечения, даже если оно финансируется частным образом, и есть некоторые доказательства его пользы при остеоартрите тазобедренного сустава.
PRP получают путем забора небольшого образца крови пациента и подвергают его центрифугированию для отделения тромбоцитов от других компонентов крови. Полученный раствор PRP содержит высокую концентрацию тромбоцитов, факторов роста, цитокинов и других биологически активных молекул, которые, как считается, способствуют заживлению тканей. Одна из проблем заключается в том, что в литературе встречается множество различных препаратов или концентраций различных элементов крови, что затрудняет выводы о PRP как о методе лечения.
Тромбоциты играют важную роль в процессе заживления, инициируя и координируя восстановление тканей. Предполагается, что при введении тромбоцитов в поврежденную или дегенерированную область выделяемые ими факторы роста и другие биологически активные молекулы способствуют пролиферации клеток, синтезу коллагена, ангиогенезу и регенерации тканей, тем самым ускоряя заживление и уменьшая боль и воспаление. Исследования на животных показали положительные изменения в костной и хрящевой ткани в ответ на применение PRP, однако аналогичные данные на людях отсутствуют.
В обзорах, посвященных применению PRP для лечения остеоартрита тазобедренного сустава, приводятся довольно ограниченные данные о том, что
- PRP превосходит Кортизон и гиалуроновую кислоту в плане уменьшения боли через 6 месяцев после введения;
- PRP оказывает положительное влияние на функцию (WOMAC) через 3 месяца, но только в сочетании с гиалуроновой кислотой (Zhao, 2020).
В целом наблюдается вариабельность процедур, подготовки PRP и результатов, а также отсутствие четких и воспроизводимых положительных результатов. Несмотря на заманчивые перспективы заживления хряща и кости, такие эффекты пока не установлены, и в настоящее время PRP не рекомендуется ни в одном руководстве по лечению остеоартрита тазобедренного сустава или боли, связанной с ним, из-за недостаточного количества доказательств клинической эффективности (Ayhan, 2014; Probst, 2023; Berney, 2020).
Возможные риски внутрисуставных инъекций богатой тромбоцитами плазмы
Инъекции PRP в целом считаются безопасными, поскольку в них используются компоненты собственной крови пациента. Сообщалось лишь о незначительных побочных явлениях, включая временную боль и припухлость сустава (Ayhan, 2014).
Варианты, преимущества и риски периартикулярных инъекций
Периартикулярные инъекции также используются для диагностики и лечения различных заболеваний в области тазобедренного сустава, чаще всего для лечения тендинопатии или «бурсита», периферических невропатий или мышечной боли, связанной с внесуставным ущемлением. Что касается суставной боли, то наиболее распространенными препаратами являются местные анестетики и Кортизон, а процедура PRP появилась совсем недавно.
Показания и преимущества периартикулярных инъекций местного анестетика
Инъекции местного анестетика в мягкие ткани, располагающиеся вокруг тазобедренного сустава, обычно используются либо с диагностической целью, либо для уменьшения боли. Инъекции местного анестетика с диагностической целью должны выполняться под контролем визуализации.
Поскольку местные анестетики имеют короткий период действия (1,6-3,5 часа), для лучшего эффекта их обычно комбинируют с кортикостероидами. Даже если кортикостероид используется в основном в диагностических целях, его часто комбинируют с местным анестетиком, чтобы добиться двойного эффекта — диагностики и лечения. Потенциальные преимущества таких инъекций должны быть сопоставлены с возможными негативными последствиями для здоровья тканей.
Возможные риски при периартикулярном введении местного анестетика
Инъекции местных анестетиков вокруг сухожилий регулярно выполняются для диагностики и лечения боли. Подобно воздействию на клетки хряща, исследования in vitro продемонстрировали цитотоксическое действие местных анестетиков, таких как Лидокаин и Бупивакаин, на теноциты (клетки сухожилий) (Zhang, 2023). Эффект опять же зависит от выбора препарата, его концентрации и времени действия.
Как и в случае с хондротоксическим действием, комбинация местного анестетика и кортикостероида, скорее всего, окажет более сильное токсическое воздействие на ткани сухожилия.
Zhang и соавт. (2023) считают, что во избежание сопутствующих побочных эффектов при использовании местных анестетиков следует тщательно подбирать препараты, их концентрацию и время действия, при этом наименьшее токсическое воздействие на сухожилия оказывает 0,2% раствор Ропивакаина.
Местные анестетики также оказывают токсическое воздействие на мышечные клетки, причем более сильное повреждение опять-таки связано с более высокими концентрациями и экспозицией. Лидокаин, Ропивакаин и Бупивакаин были связаны с миотоксичностью, причем эффект возрастал от Лидокаина к Бупивакаину (Zhang, 2023).
Наибольшему воздействию подвергаются мышечные клетки, расположенные ближе всего к месту инъекции: саркоплазматический ретикулум растворяется и дегенерирует, а в миоцитах в течение нескольких часов наблюдаются отек и некроз. Такое воздействие на мышечные клетки полностью обратимо, регенерация завершается через 3-4 недели (Zhang, 2023). Однако в некоторых случаях предусматриваются повторные инъекции через регулярные промежутки времени. Это может означать, что до восстановления тканей область будет подвергаться дальнейшему воздействию миотоксического анестетика. Негативные последствия такой инъекционной терапии неясны.
Показания и преимущества периартикулярных инъекций кортизона
Инъекции кортизона регулярно назначаются при заболеваниях мягких тканей, располагающихся вокруг тазобедренного сустава — чаще всего при тендинопатии ягодичных мышц и сопутствующем «бурсите большого вертела» (употребление кавычек здесь обусловлено тем, что истинный воспалительный процесс до сих пор не установлен), а также при тендинопатии проксимального сухожилия хамстрингов и сопутствующем «ишиальном/ишиоглютеальном бурсите».
В области передней поверхности тазобедренного сустава инъекции кортикостероидов обычно используются для дифференциальной диагностики боли, связанной с подвздошно-поясничной мышцей, и боли, связанной с тазобедренным суставом, а также для лечения боли, связанной с подвздошно-поясничной мышцей, и бурситом подвздошно-поясничной мышцы. Иногда препарат вводят в бурсу или вокруг сухожилия подвздошно-поясничной мышцы, а при некоторых подходах — внутрь влагалища сухожилия.
Инъекции кортикостероидов также используются, если есть подозрение, что источником боли является сухожилие прямой мышцы бедра.
Недавно было описано применение инъекций кортикостероидов для лечения боли и воспаления четырехглавой мышцы бедра у пациентов с внесуставным ишиофеморальным импинджментом (Liou, 2023).
Другим наиболее распространенным показанием для введения кортикостероидов является невропатическая боль, связанная с ущемлением периферических нервов.
Чаще всего инъекции кортикостероидов при невралгии вокруг бедра назначаются при:
- раздражении седалищного нерва в глубоком ягодичном пространстве (синдром глубокой ягодичной боли или синдром грушевидной мышцы);
- невралгии полового нерва, обычно ущемляющегося в канале Алкока;
- парестезии, связанные с латеральным кожным нервом бедра;
- ущемление или раздражение других мелких нервов в паховой области или нижней части живота — подвздошно-подчревного, подвздошно-пахового, бедренно-полового нервов.
Несмотря на то, что для многих из этих состояний доказательства представлены только в виде исследований/серий случаев или описаний методик, существует достаточное количество доказательств, оценивающих целесообразность инъекций кортикостероидов при лечении тендинопатии ягодичных мышц.
Эффективность инъекций кортикостероидов при тендинопатии ягодичных мышц или болевом синдроме большого вертела
Результаты различных исследований сходятся в том, что люди с тендинопатией ягодичных мышц или болевом синдроме большого вертела, скорее всего, получат хотя бы некоторую пользу от инъекций кортикостероидов в плане уменьшения боли и сопутствующих функциональных улучшений, причем наибольший эффект будет достигнут в краткосрочной перспективе. Было показано, что введение кортикостероидов превосходит обычное лечение и выжидательную тактику как в краткосрочной, так и в долгосрочной перспективе, если оценивать выраженность боли и функциональные показатели (Mellor, 2018; Wang, 2022).
Однако, введение кортикостероидов не дает преимуществ по сравнению с выжидательной тактиков в отношении качества жизни ни в краткосрочной, ни в долгосрочной перспективе, ни через 12 месяцев, когда была собрана глобальная оценка изменений (GROC) (Mellor, 2018). В одном из исследований также было показано, что в отношении интенсивности боли не было существенной разницы между кортикостероидами и плацебо в виде инъекции физраствора ни в краткосрочной (4 недели), ни в долгосрочной перспективе (6 месяцев) (Nissen, 2019).
В рандомизированном клиническом исследовании LEAP, проведенном для сравнения с современным подходом к обучению и физическим упражнениям (EDX), EDX оказался значительно более успешным, чем применение кортикостероидов, как в краткосрочной, так и в долгосрочной перспективе, что оценивалось по глобальной оценке изменений. Тяжесть и постоянство боли (% времени, когда боль присутствовала в течение последней недели) в краткосрочной перспективе, а также постоянство боли в долгосрочной перспективе были ниже в группе EDX (Mellor, 2018).
Качество жизни также значительно улучшилось в группе EDX по сравнению с группой кортикостероидов в краткосрочной и долгосрочной перспективе. Таким образом, похоже, что, несмотря на то, что кортикостероиды могут оказывать некоторое долгосрочное влияние на выраженность боли, уровень качества жизни и общее улучшение состояния людей остаются более низкими по сравнению с теми пациентами, кто придерживается плана управления нагрузкой и физических упражнений (Mellor, 2018).
В клинической практике эффект кортикостероидов, как правило, непродолжителен, и необходимо взвесить пользу от их применения и возможные побочные эффекты.
Возможные риски при периартикулярном введении кортикостероидов
Кортикостероиды токсичны для сухожилий, что может негативно отразиться на их здоровье и привести к снижению жизнеспособности клеток, их пролиферации и синтеза коллагена, а также к дезорганизации и некрозу коллагена (Dean BJF, 2014). Кортикостероиды обычно используются в паре с местными анестетиками, которые также являются тенотоксичными, что усиливает взаимный эффект.
Эти неблагоприятные эффекты на механические свойства и клеточную функцию сухожилий могут способствовать ухудшению долгосрочных результатов инъекций кортизона, даже если они сочетаются с более эффективными активными мероприятиями.
Такое воздействие может также снизить эффект от более эффективных в других случаях физических упражнений. В общей врачебной практике пациентам с тендинопатией ягодичных мышц обычно назначают кортикостероиды и дают направление на физическую терапию. Предполагается, что кортикостероиды уменьшит боль, что позволит более эффективно проводить реабилитацию. Однако, на самом деле все может быть наоборот — кортикостероиды могут отсрочить или снизить результаты программы лечебных упражнений (Coombes, 2013).
В настоящее время нет данных, подтверждающих это предположение в отношении тендинопатий области тазобедренного сустава, но при аналогичной тендинопатии для верхней конечности, в частности, латерального эпикондилита, добавление корстикостероидов к активному вмешательству приводило к более позднему и плохому результату, чем если бы пациент выполнял только упражнения (Coombes, 2013).
Это может быть обусловлено сочетанием биологических (снижение здоровья тканей) и психологических/поведенческих эффектов. Быстрое уменьшение боли после инъекции кортикостероида и местного анестетика часто приводит к снижению комплаентности в плане управления нагрузкой и физическим упражнениям. Это может способствовать ухудшению результатов и возвращению к повторным инъекциям.
Инъекции кортикостероидов, разрыв сухожилия и риск неудачных нехирургических и хирургических вмешательств
В настоящее время в научной литературе нет данных, которые бы подробно рассматривали взаимосвязь между введением кортикостероидов, разрывом сухожилия и риском неудачных нехирургических и хирургических вмешательств при тендинопатии ягодичных мышц и тендинопатии проксимального сухожилия хамстрингов.
В хирургических исследованиях, посвященных восстановлению сухожилия ягодичных мышц, участникам обычно делали несколько инъекций кортикостероидов перед операцией. Неудивительно, верно? Если они не смогли пройти реабилитационную программу или им была предложена только пассивная терапия, то почти наверняка им будет предложено введение кортикостероидов, по крайней мере, однократное (а обычно это происходит несколько раз), прежде чем будет рассмотрен вопрос об операции.
Это понятно, но здесь возникает вопрос: «Что первично, курица или яйцо?». Что было выбрано в качестве первой линии лечения — кортикостероиды или обучение пациентов и физические упражнения? Если сначала будет предложено введение кортикостероидов или кортикостероиды вместе с реабилитацией, ограничит ли эта вариация возможность достижения приемлемого для пациента результата, что приведет к повторному введения кортикостероидов, что еще больше увеличит вероятность ухудшения состояния тканей и снизит шансы на успех консервативного лечения?
Не приведет ли это к зацикливанию спирали разрушения и дисфункции тканей, что для некоторых может закончиться разрывом сухожилия и хирургическим вмешательством. Может ли воздержание от введения кортикостероидов снизить риск такого развития событий?
И снизит ли такое плохое состояние тканей на этапе операции шансы на хороший исход операции или увеличит риск повторного разрыва сухожилия? Если говорить про тазобедренный сустав, то это достоверно неизвестно, но если говорить про восстановление ротаторной манжеты плеча, то в одном систематическом обзоре было показано, что предоперационное введение кортикостероидов повышает риск ревизионной операции, если препараты вводятся в течение предшествующих 6-12 месяцев. Частота ревизий была наиболее высокой, если пациенты получали 2 и более инъекций в течение года, предшествовавшего операции.
Этот вопрос остается спорным, как и ключевой вопрос, лежащий в основе всей этой неопределенности: «Какое количество кортизона вводить безопасно?» Общий ответ медиков звучит примерно так: «2-3 раза в год». На самом деле никто не знает, какое количество введений безопасно. Вероятно, порог безопасности для разных людей и на разных стадиях патологии может быть разным. Поэтому у нас нет адекватных рекомендаций, которые позволили бы дать пациентам научно обоснованную рекомендацию.
По крайней мере, в отношении лечения тендинопатии ягодичных мышц у нас есть четкие высококачественные доказательства того, что подход, основанный на обучении и физических упражнениях, превосходит инъекции кортикостероидов. Учитывая этот факт, а также неопределенность в отношении безопасности кортикостероидов и возможного негативного влияния на результаты реабилитации, наша настоятельная рекомендация — сначала обучение и упражнения!
Повторные инъекции в мягкие ткани при болях в сухожилиях, мышцах или нервах также могут привести к некрозу подкожно жировой клетчатки и атрофии мышц.
Периартикулярные инъекции богатой тромбоцитами плазмы
Показания и преимущества периартикулярных инъекций богатой тромбоцитами плазмы при тендинопатиях тазобедренного сустава
Эффективность PRP для лечения тендинопатий изучалась, но в случае тендинопатии ягодичных мышц или болевого синдрома большого вертела данные ограничены. При тендинопатии в целом отмечается положительный эффект, хотя дизайн исследований, малый объем выборки и большое разнообразие методов приготовления PRP затрудняют интерпретацию полученных данных (Miller, 2017).
В одном из исследований, в котором сравнивались эффекты PRP, богатой лейкоцитами, и инъекций кортикостероидов, было установлено, что PRP обеспечивает статистически значимое клиническое улучшение по сравнению с инъекциями кортикостероидов через 12 недель, однако контрольной группы не было, и обе группы получали домашнюю программу консультаций и физических упражнений (Fitzpatrick, 2019). За этой когортой следили в течение 24 месяцев, но уже не в качестве рандомизированного контролируемого исследования. Тем, у кого не было положительного результата от введения кортикостероидов, через 12 недель было предложено PRP. В настоящее время имеются ограниченные данные, свидетельствующие о том, что PRP может быть более эффективна, чем кортикостероиды, в среднесрочной и долгосрочной перспективе. Однако без контрольной группы и при наличии самостоятельного обучения и программы упражнений неясно, будет ли этот эффект выше, чем при простом консультировании и самостоятельной программе упражнений или при выжидательной тактике.
Недавний систематический обзор вмешательств при тендинопатии проксимального сухожилия хамстрингов не выявил доказательств высокого или умеренного качества в отношении инъекций богатой тромбоцитами плазмы, что опять же делает их роль неопределенной (Nasser, 2021).
Необходимы дополнительные данные для уточнения роли PRP в лечении тендинопатий тазобедренного сустава и того, на каком этапе PRP может быть использована наиболее целесообразно.
Возможные риски инъекций богатой тромбоцитами плазмы при тендинопатиях тазобедренного сустава
В исследованиях на людях побочные реакции были отмечены как слабые и нечастые. PRP не обладает таким недостатком, как токсическое действие местных анестетиков и кортикостероидов. Однако до сих пор нет полного представления о вариабельности клеточных реакций, вызываемых различными препаратами PRP и на разных стадиях патологии сухожилий.
В одном из исследований in vivo было показано, что одна из форм PRP (богатая лейкоцитами PRP) может быть вредна для стволовых клеток сухожилия (Zhang, 2016). В недавнем обзоре исследований in vitro и животных моделей in vivo по оценке влияния PRP на сухожилия было отмечено, что L-PRP оказывает некоторое потенциальное положительное влияние на заживление сухожилий по сравнению с контролем, но это, по-видимому, зависит от времени — препарат помогает на ранних стадиях заживления сухожилий, но потенциально вредит на поздних стадиях заживления (Liu, 2022).
Эти животные модели предполагают хирургическое или химическое повреждение сухожилия, поэтому трудно сказать, действительно ли они отражают процессы, происходящие в пораженном сухожилии у человека. Для того чтобы понять, можно ли рекомендовать PRP для лечения тендинопатий тазобедренного сустава и на какой стадии, необходимы дальнейшие исследования.
Заключение
Что же в итоге? Не хотелось бы повторяться, но обучение и упражнения — это то, с чего необходимо начинать лечение!
Хотя местные анестетики могут использоваться в диагностике, эти препараты являются цитотоксичными, а введение препаратов под навигацией может сопровождаться ионизирующим излучением. Мы, как медицинские работники, обязаны обладать наилучшими навыками клинической диагностики, чтобы избежать ненужных диагностических инъекций (которые не всегда являются высокоточными).
Кортикостероиды, особенно в сочетании с местной анестезией (что часто встречается в клинической практике), токсичны для всех тканей опорно-двигательного аппарата. Поэтому они не должны предлагаться в качестве первой линии лечения при боли в тазобедренном суставе или окружающих мягких тканя. Мы не знаем, насколько это безопасно, а тех, кто подвержен риску более разрушительных побочных реакций, легко просмотреть. Поэтому давайте проявим осторожность и сведем к минимуму использование инъекций кортикостероидов.
Вискосуппозиции и PRP обладают заманчивыми потенциальными преимуществами на биологическом уровне, однако доказательств in-vivo на людях и четких доказательств клинического эффекта пока нет. Необходимы дальнейшие исследования, прежде чем их можно будет широко рекомендовать. Пациенты должны быть ознакомлены с имеющимися данными, которые помогут им принять обоснованное решение и взвесить риски, которые, вероятно, ниже, чем при инъекциях кортикостероидов или даже местной анестезии. Будем следить за развитием исследований!