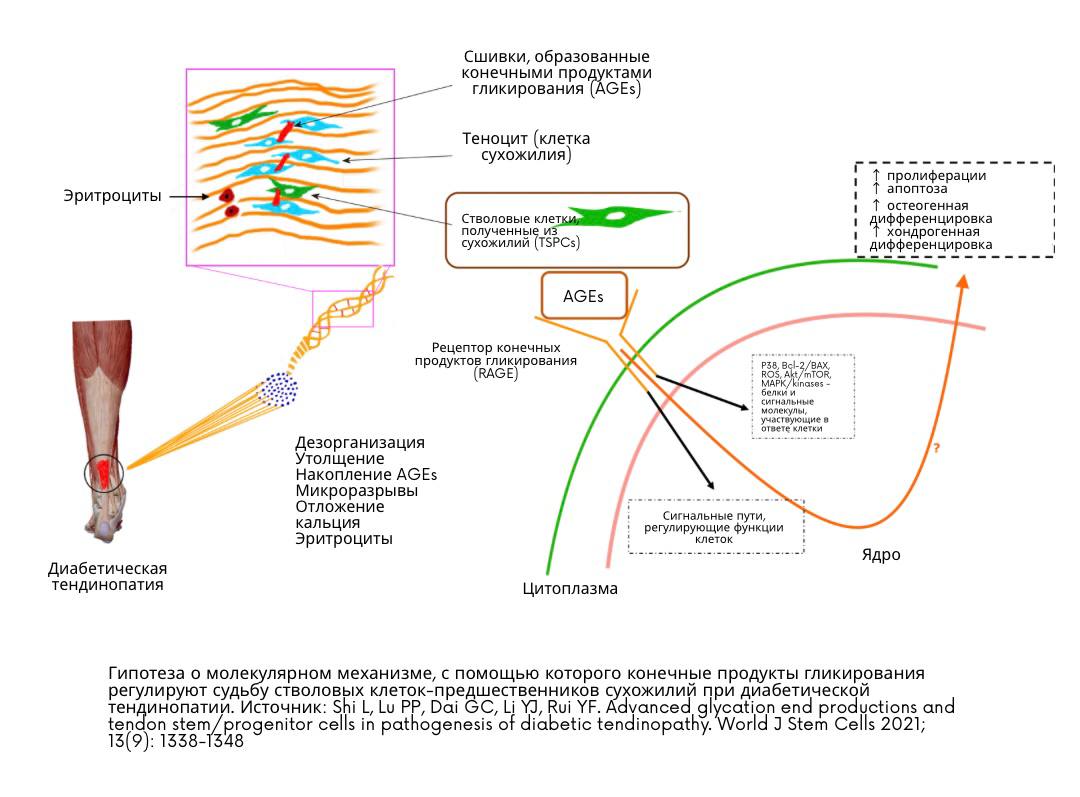
Нарушения ходьбы встречаются примерно у 80% пациентов, перенесших инсульт, становясь основным препятствием для социальной интеграции и выполнения повседневной деятельности.
Восстановление ходьбы является одной из основных целей программ реабилитации и часто становится главным приоритетом для самих пациентов. Хотя большинство людей восстанавливают базовую способность к передвижению, многие из них не достигают требуемых параметров, необходимых для полноценного и независимого выполнения повседневных активностей. Падения остаются серьезной проблемой для этой категории пациентов.
Современная парадигма реабилитации смещается от пассивных методик и компенсаторных стратегий к активным, высокоинтенсивным и технологически насыщенным интервенциям, основанным на принципах доказательной медицины и глубоком понимании механизмов нейропластичности.
Патофизиологические основы нарушений ходьбы после инсульта
Развитие синдрома центрального гемипареза вследствие перенесенного инсульта приводит к формированию патологического стереотипа ходьбы, который представляет собой комбинацию следующих факторов:
- Изменения мышечного тонуса.
- Снижение мышечной силы.
- Изменения длины мягких тканей.
- Сенсорные нарушения.
- Нарушения временных параметров цикла ходьбы.
- Снижение скорости ходьбы.
- Нарушения баланса.
- Нарушения визуального сканирования.
- Когнитивные нарушения.
Биомеханический анализ гемипаретической походки
Понимание кинематических и кинетических отклонений необходимо для постановки специфических терапевтических целей.
Типичная гемипаретическая походка включает в себя снижение скорости ходьбы, уменьшение частоты шагов и сокращение длины шага на паретичной стороне. Пациенты проводят значительно больше времени в фазе опоры на сохранной конечности, стремясь минимизировать нагрузку на пораженную сторону.
| Характеристика походки | Паретичная конечность | Сохранная конечность | Биомеханическое последствие |
| Время опоры | Снижено | Увеличено | Повышенная нагрузка на суставы сохранной стороны |
| Время переноса | Увеличено | Снижено | Нарушение ритмичности и баланса |
| Пропульсивный импульс | Резко снижен | Повышен (компенсаторно) | Снижение общей скорости и экономичности ходьбы |
Патологическая походка при инсульте характеризуется выраженной асимметрией, нарушением фазовой структуры шага, снижением темпа и патологическими синергиями.
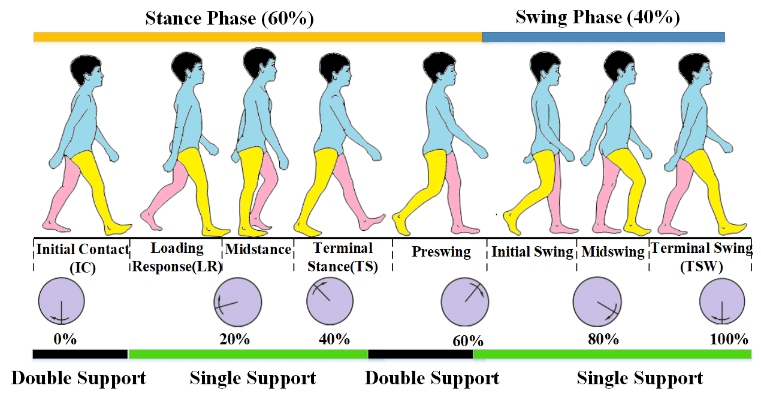
Фаза опоры (Stance Phase)
- Нестабильность коленного сустава: проявляется либо в избыточном сгибании (слабость квадрицепса), либо в рекурвации (Genu recurvatum) из-за спастичности икроножной мышцы или слабости проксимальных отделов.
- Эквиноварусная деформация: приводит к контакту с опорой всей стопой (Flat foot contact) или носком, ограничивая перекат.
- Сокращение времени опоры на паретичную конечность, что ведет к уменьшению длины шага здоровой ноги.
Фаза переноса (Swing Phase)
- Недостаточный клиренс стопы: обусловлен синдромом «свисающей стопы» (Foot drop) и снижением амплитуды сгибания в коленном и тазобедренном суставах.
- Компенсаторные стратегии:
- Циркумдукция (Circumduction): дугообразный вынос ноги через сторону.
- Хип-хайкинг (Hip hiking): элевация полутаза на стороне пареза.
- Волтинг (Vaulting): подъем на носок сохранной ноги для облегчения переноса паретичной.
Теория трех перекатов стопы при инсульте
Цикл ходьбы в норме включает три последовательных переката (rockers), каждый из которых выполняет специфическую функцию продвижения и амортизации. При инсульте эта последовательность нарушается:
- Первый перекат (Heel Rocker): В норме начинается с удара пяткой. При парезе тыльных сгибателей стопа опускается плашмя или касается пола носком, что исключает фазу амортизации и приводит к избыточной нагрузке на коленный сустав.
- Второй перекат (Ankle Rocker): Продвижение голени над фиксированной стопой. Спастичность икроножной мышцы или использование жестких ортезов блокирует это движение, вызывая преждевременный отрыв пятки или гиперэкстензию колена (genu recurvatum).
- Третий перекат (Forefoot Rocker): Фаза отталкивания. Снижение силы подошвенных сгибателей и нарушение проприоцепции делают невозможным эффективный перенос веса на передний отдел стопы, что заставляет пациента компенсировать дефицит за счет избыточного сгибания в тазобедренном суставе.
Диагностика
Для объективизации статуса и оценки динамики рекомендуется использовать валидированные инструменты:
| Инструмент | Параметр оценки | Клиническая значимость |
| 10-метровый тест (10MWT) | Скорость ходьбы | Прогноз социальной интеграции (<0.4 м/с — домашний уровень; >0.8 м/с — общественный) |
| 6-минутный тест (6MWT) | Функциональная выносливость | Оценка кардиореспираторного резерва и толерантности к нагрузке |
| Тест TUG (Timed Up & Go) | Динамический баланс | Риск падений и мобильность при смене положений |
| Шкала FAC (Functional Ambulation Categories) | Уровень зависимости | Определение потребности в физической помощи или средствах опоры (от 0 до 5) |
Читайте также статью: Тесты для пациентов с инсультом.
Нейропластичность как биологический субстрат восстановления ходьбы
Успех тренировки ходьбы напрямую зависит от способности центральной нервной системы к структурной и функциональной реорганизации. Процесс нейропластичности включает в себя синаптическое масштабирование, аксональный спраутинг и рекрутирование окружающих нейронных сетей. Центральную роль в этом процессе играет нейротрофический фактор головного мозга (BDNF), который выступает медиатором долгосрочной потенциации и выживания нейронов.
Роль BDNF и метаболического прайминга
Исследования последних лет подчеркивают значение интенсивности физической нагрузки для модуляции уровней BDNF. Аэробные упражнения высокой интенсивности стимулируют высвобождение лактата, который проникает через гематоэнцефалический барьер и активирует сигнальные пути, ответственные за экспрессию гена BDNF. Этот механизм лежит в основе концепции «аэробного прайминга»: кратковременная высокоинтенсивная нагрузка перед основной тренировкой навыка ходьбы «подготавливает» мозг к усвоению новых двигательных паттернов.
| Механизм прайминга | Влияние на нейропластичность | Клиническое значение |
| Увеличение концентрации BDNF | Поддержка синаптической пластичности и роста дендритов | Улучшение долгосрочного удержания двигательного навыка |
| Снижение интракортикального торможения | Облегчение активации паретичных мышечных групп | Ускорение рекрутирования двигательных единиц |
| Повышение кортикоспинальной возбудимости | Усиление ответа на афферентные стимулы | Снижение порога произвольной инициации движения |
Помимо BDNF, важную роль играет фактор роста эндотелия сосудов (VEGF), который способствует ангиогенезу в периинфарктной зоне, обеспечивая трофическую поддержку восстанавливающимся нейронам. Снижение уровней BDNF в плазме крови в остром периоде ассоциировано с худшим прогнозом восстановления мобильности, что делает интенсивную физическую терапию необходимым условием для нормализации нейротрофического профиля.
Критическое окно и перинейрональные сети
Период максимальной пластичности мозга после инсульта ограничен во времени. Экспериментальные данные указывают на существование «критического окна», характеризующегося временным снижением плотности перинейрональных сетей (PNN) — структур внеклеточного матрикса, которые в норме стабилизируют синапсы и препятствуют их перестройке. В подостром периоде (до 4–6 недель) наблюдается естественное снижение ингибирующих сигналов от парвальбумин-позитивных интернейронов, что создает уникальную возможность для переобучения. Промедление в инициации интенсивных тренировок ходьбы в этот период приводит к преждевременной стабилизации патологических паттернов и ограничению функционального потенциала.
Принципы реабилитации после инсульта (CSBPR 2025)
Успешная реабилитационная программа основывается на нескольких фундаментальных принципах:
- Специфичность задачи: Тренировка должна быть направлена на конкретную цель (например, дойти до магазина), быть значимой для пациента и прогрессивно усложняться.
- Аэробный компонент: Рекомендуется проведение аэробных тренировок 3–5 раз в неделю продолжительностью 20–60 минут. Скрининг сердечно-сосудистой системы перед началом таких программ является обязательным.
- Использование слуховых стимулов: Ритмическая слуховая стимуляция (RAS) должна применяться для улучшения темпа и симметрии ходьбы, особенно у пациентов с выраженными нарушениями ритма.
- Вовлечение семьи: Обучение лиц, осуществляющих уход, и их участие в тренировках повышает приверженность пациента к реабилитации и обеспечивает безопасность при выполнении домашних упражнений.
Эволюция подходов к восстановлению ходьбы демонстрирует движение от интуитивных методов к строгим научным протоколам. Основной задачей физического терапевта сегодня является не только помощь в передвижении, но и создание условий для эффективной нейропластической реорганизации мозга пациента. Высокая интенсивность, использование современных технологий и регулярный мониторинг функциональных показателей — это три столпа, на которых строится успешная реабилитация ходьбы в XXI веке.
Терапевтические стратегии
Существует множество подходов к тренировке ходьбы у пациентов после инсульта, каждый из которых имеет свои особенности, показания и эффективность.
Конвенциональная тренировка ходьбы
Конвенциональная тренировка ходьбы включает упражнения на твердой поверхности под наблюдением терапевта. Это может включать тренировку ходьбы с поддержкой, упражнения на равновесие, тренировку подъема по лестнице и тренировку, ориентированную на решение конкретной задачи (Task-Specific Training), тренировку с двойными задачами (Dual-tasking). Сравнительные исследования показывают, что конвенциональная тренировка ходьбы может быть столь же эффективной, как и тренировка на беговой дорожке с частичной разгрузкой веса тела (BWSTT), хотя результаты могут варьироваться в зависимости от стадии восстановления пациента. Исследование с участием 40 пациентов показало, что BWSTT и конвенциональная терапия имеют сопоставимую клиническую эффективность.
Тренировка на беговой дорожке с частичной разгрузкой веса тела (Body Weight Supported Treadmill Training — BWSTT)
BWSTT позволяет пациентам тренировать ходьбу с частичной разгрузкой веса тела, что снижает нагрузку на пораженную конечность и дает возможность начинать тренировку на более ранних этапах реабилитации. В рандомизированном контролируемом исследовании с участием 97 пациентов в подостром периоде инсульта сравнивали BWSTT с конвенциональной тренировкой ходьбы по твердой поверхности. После 4 недель тренировок все пациенты обеих групп смогли самостоятельно передвигаться, при этом статистически значимых различий между группами не наблюдалось ни сразу после лечения, ни через 6 месяцев наблюдения.
Проприоцептивная нейромышечная фасилитация (Proprioceptive Neuromuscular Facilitation — PNF)
Применение PNF в тренировке ходьбы, особенно при подъеме по лестнице, может значительно улучшить баланс у пациентов с инсультом. В исследовании с участием 30 пациентов группа, проходящая тренировку ходьбы по лестнице с применением PNF, показала статистически значимое улучшение по шкале Берга (BBS) и функциональному тесту на дотягивание (FRT), а также снижение времени в тесте «Встань и иди» (TUG) по сравнению с контрольной группой.
Тренировки с биологической обратной связяю (БОС)
Технология биологической обратной связи для тренировки функции ходьбы оценивается как эффективная и перспективная, особенно для пациентов в раннем восстановительном периоде после инсульта. Основные параметры тренировки с использованием БОС включают скорость ходьбы, длину цикла шага и каденс (частоту шагов). Используются различные технические способы представления обратной связи: зрительный, слуховой или их комбинация. Исследование с 12 пациентами показало, что целенаправленная БОС-тренировка по гармонизации фазы опоры позволяет снижать функциональную асимметрию по данному параметру и оказывает положительный эффект на другие показатели цикла ходьбы.
Роботизированная тренировка ходьбы (RAGT)
Роботизированные системы обеспечивают высокоинтенсивную повторяемую практику, которую трудно достичь при ручном содействии терапевтов. Однако эффективность RAGT зависит от типа устройства и фазы инсульта. Системы с энд-эффекторами (например, G-EO, GaitTrainer) демонстрируют более выраженные результаты в восстановлении скорости ходьбы и баланса по сравнению с экзоскелетными системами (например, Lokomat). Это связывают с тем, что энд-эффекторы позволяют сохранять большую свободу движений в проксимальных суставах и обеспечивают более естественную стимуляцию подошвенных рецепторов.
Критически важным является время начала RAGT. Мета-анализы подтверждают наибольшую эффективность робототехники в подостром периоде (от 7 дней до 6 месяцев). В последующем роботы могут быть полезны для поддержания мобильности, но их влияние на функциональный прирост значительно ниже из-за сниженного нейропластического потенциала.
Ортезирование и функциональная электростимуляция
Коррекция свисающей стопы и нестабильности колена требует индивидуального подхода к выбору вспомогательных устройств. Клиническая дискуссия часто ведется вокруг выбора между голеностопными ортезами (AFO) и функциональной электростимуляцией (FES).
Сравнительная эффективность AFO и FES
Современные клинические рекомендации указывают на отсутствие явного превосходства одного метода над другим в плане мгновенного влияния на скорость ходьбы, однако FES обладает рядом долгосрочных преимуществ.
- Ортопедический эффект: AFO обеспечивает стабильную механическую поддержку, предотвращая инверсию стопы. Однако жесткие модели могут ограничивать работу мышц голени, способствуя их атрофии.
- Терапевтический эффект: FES стимулирует активное сокращение мышц в нужную фазу шага, что способствует укреплению мышечного корсета и формированию новых кортикоспинальных путей. Исследования подтверждают наличие «эффекта последействия» (carry-over effect): после прекращения использования FES пациент сохраняет лучшие показатели ходьбы, чем до тренировок.
Инновационным направлением является использование ортезов с регулируемым сопротивлением (масляные демпферы, AFO-OD). Такие устройства позволяют имитировать работу мышц-эксцентриков в фазе первого переката, обеспечивая плавное опускание стопы и предотвращая патологическую рекурвацию колена. Трехнедельный курс тренировок с использованием AFO-OD продемонстрировал статистически значимое улучшение кинетики голеностопного сустава даже при ходьбе без ортеза.
Силовая тренировка
Прогрессивная силовая тренировка с нагрузками 70% и более от максимальной силы является безопасным и эффективным методом для увеличения мышечной силы без негативного влияния на мышечный тонус. Увеличение мышечной силы положительно коррелирует с показателями ходьбы и воспринимаемым участием в повседневной жизни. В исследованиях отмечается, что силовая тренировка также может служить эффективной формой фитнес-тренировки для пациентов с минимально выраженной мышечной слабостью.
Перспективные комбинированные и современные подходы
Исследования 2024-2025 годов изучают комбинированные и инновационные методы для потенцирования эффектов реабилитации:
Высокоинтенсивная тренировка ходьбы (High-Intensity Gait Training — HIGT)
Наиболее значимым изменением в клинических рекомендациях последних лет стало признание эффективности высокоинтенсивной тренировки ходьбы. HIGT фокусируется на достижении большого объема практики в сочетании с умеренно-высокой аэробной нагрузкой.
Согласно обновленным данным, включая результаты масштабных исследований в Канаде, для запуска нейропластических изменений требуется достижение определенных пороговых значений нагрузки во время сессии.
| Параметр | Целевое значение | Метод контроля |
| Частота сердечных сокращений (ЧСС) | 70–85% от HRmax | Пульсометрия в реальном времени |
| Объем ходьбы | > 2000 шагов за сессию | Шагомеры или носимые датчики |
| Частота занятий | 5 дней в неделю | Дневник тренировок |
| Длительность активной фазы | 30–45 минут | Секундомер |
Исследование, охватившее 306 пациентов в подострой фазе инсульта, продемонстрировало, что прогрессивное увеличение интенсивности ходьбы (достижение 2000 шагов за 30 минут) приводит к увеличению дистанции в тесте 6-минутной ходьбы на 43.6 метра по сравнению с контрольной группой, получавшей стандартную терапию. Это улучшение коррелирует с повышением качества жизни и уровня повседневной активности.
HIGT не ограничивается монотонной ходьбой по беговой дорожке. Ключевым компонентом является вариативность условий: ходьба с разной скоростью, преодоление препятствий, подъем по лестнице и изменение направления движения. Такая практика заставляет мозг постоянно адаптироваться к изменяющимся условиям среды, что способствует формированию более устойчивого и адаптивного двигательного навыка. Важно, что терапевт должен допускать определенную степень ошибок в движениях пациента, так как «ошибочное обучение» (error-based learning) является мощным стимулом для коррекции внутренних моделей движения в мозге.
Виртуальная реальность (VR) и когнитивно-моторное взаимодействие
Виртуальная реальность предоставляет возможность тренировки ходьбы в контексте сложных поведенческих сценариев, которые трудно воспроизвести в клинике. Использование VR повышает мотивацию пациента и позволяет интегрировать когнитивную нагрузку в процесс ходьбы (например, навигация в виртуальном супермаркете).
Полностью иммерсивные системы (HMD) обеспечивают глубокое погружение, однако исследования показывают, что полуиммерсивные системы (проекции на экран перед беговой дорожкой) могут быть предпочтительнее для пациентов с нарушениями баланса, так как они сохраняют визуальный контакт с реальной опорой. Мета-анализ 2025 года выявил, что VR-программы продолжительностью более 20 сессий значимо улучшают динамическую стабильность и снижают риск падений.
Сочетание роботизированной тренировки ходьбы с транскраниальной магнитной стимуляцией (ТМС)
Пилотные рандомизированные контролируемые исследования показывают, что такое сочетание может оказывать положительное влияние на параметры ходьбы и баланса у пациентов с инсультом.
Функциональная диагностика и мониторинг прогресса
Адекватная оценка состояния пациента является фундаментом реабилитационного процесса. Традиционное использование шкалы баланса Берга (BBS) подвергается критике из-за недостаточной чувствительности к изменениям у амбулаторных пациентов.
Преимущества шкалы Функциональной оценки ходьбы (FGA)
Шкала FGA, являющаяся модификацией Динамического индекса ходьбы (DGI), была разработана для оценки баланса во время выполнения сложных локомоторных задач. Она включает 10 пунктов, оцениваемых по 4-балльной шкале (от 0 до 3), с максимальным баллом 30.
- Чувствительность: В отличие от BBS, FGA не имеет выраженного «эффекта потолка» и позволяет выявлять невыраженные нарушения координации у пациентов с высокой скоростью ходьбы.
- Валидность: Оценка по FGA сильно коррелирует со скоростью ходьбы (r = 0.82) и индексом Бартел (r = 0.71).
- Прогностическая ценность: Пороговое значение ≤ 20/30 баллов служит надежным индикатором высокого риска падений у пациентов после инсульта.
Для более глубокого анализа в современных клиниках применяются системы видеоанализа движений и носимые инерциальные датчики (IMU). Эти технологии позволяют количественно оценить углы в суставах и симметрию шага в условиях реальной среды, что критически важно для оценки переноса навыков из клиники в повседневную жизнь.
Заключение
Восстановление ходьбы после инсульта — это сложный многоэтапный процесс, включающий как спонтанное восстановление, так и эффекты целенаправленных терапевтических вмешательств. Эффективная реабилитация требует строго индивидуализированного подхода с учетом специфических нарушений и потенциала каждого пациента, а также рациональной комбинации различных методов тренировки. Несмотря на разнообразие и постоянное развитие доступных методов тренировки ходьбы — от конвенциональных до высокотехнологичных (роботизированных, с БОС и FES) — необходимы дальнейшие исследования для оптимизации протоколов лечения, определения наиболее эффективных и экономически целесообразных комбинаций методов, а также установления четких критериев отбора пациентов для различных видов терапии. Выбор метода должен основываться не только на его технологической сложности, но и на индивидуальных характеристиках пациента, этапе реабилитации и доступных ресурсах. Обновленные клинические рекомендации подчеркивают важность ранней, интенсивной и ориентированной на решение конкретных задач реабилитации для достижения наилучших функциональных исходов.